Электролиты для гальваники: Электролиты для гальваники, цены от 500р. на электролиты в Москве
Содержание
Электролиты для гальваники, цены от 500р. на электролиты в Москве
Компания «6 микрон» предлагает купить всё для гальваники: наборы для гальваники в домашних условиях, электролиты для различных гальванических технологий таких как:
- золочение;
- меднение;
- никелирование;
- палладирование.
Мы самостоятельно производим типовые составы для гальваники купить которые можно отправив заявку на сайте. Расходные материалы протестированы.
Электролиты, с которыми мы работаем и продаем, производятся на базе нашего предприятия. Поэтому мы гарантируем качество товара!
Скачать полный прайс
| Название | Объем | Цена за ед. | Цена за 5 ед. | Более 10 ед. |
| Электролиты для золочения | ||||
| электролит золота чистый (999,9) 2/л | 1 л. | 20000 | 19500 | 19500 |
| электролит золота с кобальтом (999,0) 2/л | 1 л. | 20000 | 19500 | 19500 |
| электролит «зеленого» золота т 2г/л | 1 л. | 20000 | 19500 | 19500 |
| электролит «зеленого» золота м 2г/л | 1 л. | 20000 | 19500 | 19500 |
| электролит розового золота (585проба) 1г/л концентрат | 100 мл | 11500 | 10000 | 10000 |
| электролит для золочения карандашом 20 г/л | 100 мл | 20000 | 19500 | 19500 |
| электролит для химического золочения 2 г/л | 1 л. | 20000 | 19500 | 19500 |
| Электролиты для серебрения | ||||
| электролит для серебрения в ванне 36 г/л | 1 л. | 10000 | 9600 | 9600 |
| электролит для предварительного серебрения 5 г/л | 1 л. | 4000 | 4000 | 4000 |
| электролит для серебрения карандашом 36 г/л | 100 мл | 2500 | 2300 | 2300 |
| Электролиты других платиноидов | ||||
| электролит палладирования 2 г/л | 1 л. | 45000 | 45000 | 45000 |
| электролит белого родия 2 г/л | 1 л. | по запросу | по запросу | по запросу |
| электролит черного рутенирования 2 г/л | 1 л. | 10000 | 9000 | 9000 |
| Электролиты меднения | ||||
| электролит матового меднения сернокислый | 1 л. | 1500 | 1300 | 1300 |
| электролит блестящего меднения сернокислый | 1 л. | 1600 | 1500 | 1500 |
| электролит меднения для стали щелочной | 1 л. | 2500 | 2300 | 2300 |
| электролит меднения матовый нейтральный | 1 л. | 2500 | 2300 | 2300 |
| электролит химического меднения | 1 л. | 1000 | 900 | 900 |
| Электролиты никелирования | ||||
| электролит никелирования подслойный | 1 л. | 2000 | 1900 | 1800 |
| электролит никелирования блестящий | 1 л. | 2500 | 2300 | 2200 |
| электролит никелирования матовый серый | 1 л. | 2200 | 2100 | 2000 |
| электролит никелирования черный | 1 л. | 2400 | 2300 | 2300 |
| электролит химического никелирования кислотный | 1 л. | 1800 | 1700 | 1700 |
| электролит химического никелирования щелочной | 1 л. | 1800 | 1700 | 1700 |
| Электролиты для предварительной обработки | ||||
| электролит электрохимического обезжиривания | 1 л. | 1100 | 1000 | 900 |
| электролит химического обезжиривания | 1 л. | 1100 | 1000 | 900 |
| электролит электрохимической полировки медных сплавов | 1 л. | 1200 | 1000 | 1000 |
| электролит химической полировки медных сплавов | 1 л. | 1500 | 1500 | 1300 |
| электролит для удаления хрома и лако-красочных покрытий | 1 л. | 900 | 800 | 800 |
| электролит для химической и электрохимической активации металлов | 1 л. | 900 | 800 | 800 |
| электролит для химической активации серебра | 1 л. | 700 | 700 | 700 |
| электролит для пассивации меди и серебра | 1 л. | 900 | 800 | 800 |
| электролит для чернения меди и серебра | 1 л. | 800 | 800 | 500 |
| Электролиты для гальванопластических работ | ||||
| состав для нанесения токопроводящего слоя А | 1 л. | 2200 | 2000 | 2000 |
| состав для нанесения токопроводящего слоя В | 1 л. | 1500 | 1200 | 1000 |
| состав для активации и сенсибилизации поверхности С | 1 л. | 2000 | 1800 | 1500 |
| активатор-сенсибилизатор поверхности палладиевый совмещенный | 1 л. | 22000 | 22000 | 22000 |
| активатор поверхности серебряный | 1 л. | по запросу | по запросу | по запросу |
| Составы для удаления нежелательных покрытий | ||||
| состав для снятия нитрида титана | 1 л. | 1500 | 1500 | 1200 |
| состав для удаления никелевого покрытия с меди | 1 л. | 1500 | 1500 | 1200 |
| состав для удаления серебряного покрытия с меди | 1 л. | 1800 | 1500 | 1200 |
| состав для удаления золотых покрытий | 1 л. | 2000 | по запросу | по запросу |
| состав для удаления хромовых покрытий | 1 л. | 900 | 800 | 800 |
| Анодные материалы | ||||
| аноды медные АМФ 1 | 1 шт | 3000 | 3000 | 3000 |
| аноды никелевые НПА-1, Н0 | 1 шт | 4500 | 4500 | 4500 |
| аноды серебряные 999 | 100 гр | по запросу | по запросу | по запросу |
| аноды родированный титан | 1 кв. дм. | 9000 | 9000 | 9000 |
| Обучение технолога | ||||
| комплект «Стандарт» | 1 шт | от 55 000 | по запросу | по запросу |
| комплект «Стандарт Плюс» | 1 шт | от 70 000 | по запросу | по запросу |
| комплект «Знания — сила» | 1 шт | от 45 000 | по запросу | по запросу |
| комплект «Реставратор» | 1 шт | от 40 000 | по запросу | по запросу |
При оформлении заказа онлайн скидка 10 %!
Наш приоритет — индивидуальный подход к каждому заказу и качество выполняемых работ!
Отправить заявку или задать вопрос:
Ваше имя
Ваш e-mail
Ваш телефон *
Сообщение
Текст с картинки *
Анодные материалы
10000
Аноды для гальваники (гальванические аноды) – важная составляющая любого гальванического процесса.
 Существует два метода нанесения покрытий: электрохимический и химический. Разница…
Существует два метода нанесения покрытий: электрохимический и химический. Разница…Аноды медные
10000
В наше время, когда активное развитие получают автомобильные и энергетические отрасли, большую значимость приобретают медные аноды. В промышленности сегодня находят…
Tags: запросу
Аноды никелевые
10000
Никелевые аноды изготавливают из чистого никеля разных производителей в форме овальных и прямоугольных листов. Самыми лучшими принято считать материалы марки…
Tags: запросу
Гальваника. Рецепт электролита и работа с блоком питания. Часть 2
Живая Медь Украшения. Мария
Эта публикация является продолжением моей первой статьи по гальванике. Сегодня мы рассмотрим еще один рецепт электролита, а также работу с блоком питания.
Этот электролит я называю электролитом гладкого меднения. Методика его приготовления такая же, как любого сернокислого электролита и об этом я писала в предыдущей статье.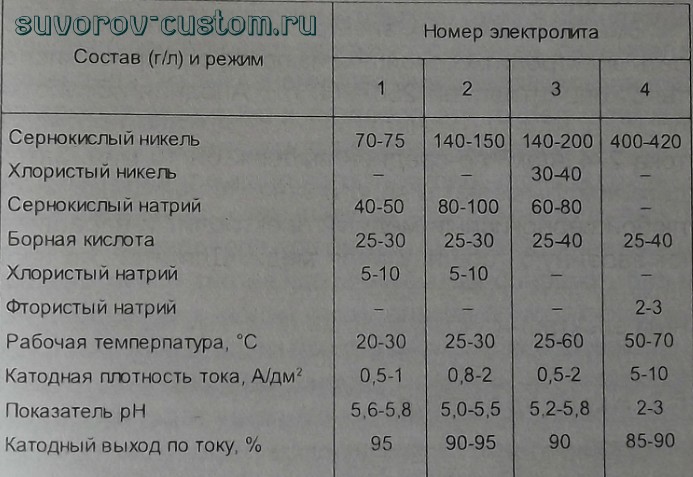 Во всех моих рецептах количество серной кислоты указано в расчете на использование автомобильного аккумуляторного электролита.
Во всех моих рецептах количество серной кислоты указано в расчете на использование автомобильного аккумуляторного электролита.
Итак, рецепт:
- 200 г медного купороса;
- 140 -145 мл серной кислоты;
- 0,07 г тиомочевины;
- 0,07 г повареной соли (мелкой «экстра»).
Плюсы данного электролита:
1) Хорошее, ровное, досточно блестящее покрытие.
2) Хорошая скорость закрытия и наращивания меди (экономит элетричество).
3) Отлично поддается любой полировке.
Минусы:
1) Достаточно чувствителен к силе тока.
2) Покрытие не слишком пластично, при попытке изменить форму может дать трещины.
При достаточном количестве тиомочевины и правильно выбранной силе тока должен получиться вот такой листик, гладкий, но имеющий на поверхности тонкую матовую пленку.
Пленка быстро убирается любой полировальной пастой
Если тиомочевины в электролите недостаточно — мы можем получить вот такую интересную мелкокрупитчатую поверхность изделия. Она чуть более блестящая, чем при матовом меднении и лучше поддается полировке. При патинировке на такой поверхности можно добиться интересного слегка перламутрового эффекта. Фото до и после полировки.
Она чуть более блестящая, чем при матовом меднении и лучше поддается полировке. При патинировке на такой поверхности можно добиться интересного слегка перламутрового эффекта. Фото до и после полировки.
А теперь поговорим о самом, пожалуй, важном — ТЕХНИКЕ БЕЗОПАСНОСТИ.
Любые работы с электролитом ОБЯЗАТЕЛЬНО, ВСЕГДА, БЕЗ ИСКЛЮЧЕНИЙ проводятся в перчатках, очках и фартуке. Сейчас буду пугать!
1. Перчатки — тонкие латексные. Буквально через несколько дней работы без перчаток начинают слоиться ногти и сглаживаться папиллярные линии на подушечках пальцев из за чего пальцы теряют чувствительность. Нам, рукодельницам, это надо?
2. Очки — строительные, плотно прилегающие к лицу. Поверьте, не раз и не два у вас будет случаться ПЛЮХ!. Кошка под ногу подвернулась, проволочка оборвалась… Химический ожог роговицы — не самое приятное переживание в жизни.
3. Фартук — прорезиненный или клеенчатый, покупается в магазине спецодежды. Электролит очень быстро прожигает дыры в одежде. За первые 2 месяца гальванических работ (еще без фартука) я потратила на домашнюю одежду больше, чем за 10 предыдущих лет. Не думайте, что вам удасться избежать случайного попадания электролита на одежду!
За первые 2 месяца гальванических работ (еще без фартука) я потратила на домашнюю одежду больше, чем за 10 предыдущих лет. Не думайте, что вам удасться избежать случайного попадания электролита на одежду!
При смешивании электролита очень желательно надеть респиратор или хотя бы влажную марлевую повязку во избежание попадания пыли медного купороса в дыхательные пути.
Гальваническую ванну лучше всего поставить на большой лист пластика. Рядом обязательно должна быть миска с водой. Вынимаем изделие, прополаскиваем в воде и прямо так, в миске, несем к раковине. Не стоит капать кислотой на ламинат.
Даже небольшая ванночка (1-2 л) должна находиться в хорошо проветриваемом помещении. Подоконник отлично подойдет.
Пожалуйста, всегда будьте внимательны и осторожны!!!! Помните, что вы работаете с опасными реактивами!!!
Ну, и в завершение, несколько слов о работе с блоком питания. Иногда люди жалуются, что изготовив по моему рецепту электролит электрохимической полировки, не получают блестящего изделия. Или что при использовании электролита матового меднения структура меди на поверхности получается крупитчатой и осыпается. Это все — ошибки в работе с блоком питания.
Или что при использовании электролита матового меднения структура меди на поверхности получается крупитчатой и осыпается. Это все — ошибки в работе с блоком питания.
Самое главное — у нас должен быть блок питания с вольтметром и амперметром.
Итак, начинаем: сначала мы наш листочек покрыли графитовым лаком в 3 слоя (не экономьте на лаке) и обратили внимание на то, что проволочная намотка на черешке листа тоже покрыта лаком.
Погружаем листочек в ванну и выставляем на БП 0,8-0,9 вольт. Ждем пока на амперметре на появится 0.13-0,15 Ампер и повышаем вольтаж до 1,1 Вольт. Опять ждем, пока на амперметре не покажется 0,35 А. Теперь повышаем вольтаж до рабочей величины.
А вот эту саму рабочую величину мы определяем эмпирически. Например, на достаточно крупный березовый лист, опущенный в электролит гладкого меднения нужно подать около 1,6 Вольт.
За полностью закрытым листом внимательно следим.
Изделие блестящее по краям, но матовое в центре — прибавить силу тока. Наоборот: изделие, блестящее в центре, но матовое по краям — силу тока убавить.
Наоборот: изделие, блестящее в центре, но матовое по краям — силу тока убавить.
При чрезмерной силе тока изделие начинает «пригорать» по краям. На кончиках листьев возникают утолщения и наплывы меди.
Можно использовать этот эффект в декоративных целях, например при изготовлении шапочек для бусин, меднении кристаллов или лэмпворка и т.д. Можно, добившись нужного эффекта, убавить силу тока, чтобы эти наплывы покрылись слоем гладкой меди, для дальнейшей полировки.
А теперь скажите мне, пожалуйста, какая тема вас больше всего интересует (чтобы я знала, о чем писать следующую статью):
1) Восстановление электролита.
2) Полировка и химическое оксидирование.
3) Электрохимическое оксидирование.
Рейтинг
★
★
★
★
★
5.0
(7 голосов)
Живая Медь Украшения. Мария
Россия, Нижний Новгород
Магазин (18)
Блог (33)
Следите за творчеством мастера
Публикации по теме
Ключевые слова
- Ключевые слова
- гальваника
- гальванопластика
- электроформинг
- гальваника дома
- гальваника начинающим
- гальваника бп
- блок питания
- медный лист
- меднение
- меднение дома
- гальванический электролит
- рецепт электролита
- гладкое меднение
- зеркальное меднение
- электролит для гальваники
- сернокислый электролит
- гальваника для начинающих
- гальваника начало
- гальванопластика начало
Рубрики публикаций
Идеи и вдохновение
Всё о продажах
Мода, стиль, тенденции
Хендмейд как бизнес
Материалы и инструменты
Организация мастерской
История рукоделия
Занимательные истории
Интервью
Хитрости и советы / Lifehack
Ответить
Проверено
215,1 тыс. + просмотров
+ просмотров
Подсказка: По сути, гальванопокрытие — это процесс нанесения одного металла на другой путем гидролиза для предотвращения коррозии металла, а также для предотвращения разложения. в этом процессе используется электрический ток для восстановления растворенных катионов металлов с целью образования плотного когерентного металлического покрытия на электроде.
Полный пошаговый ответ: Итак, прежде чем мы начнем решение, я должен сказать вам, что благородные металлы используются только в процессе гальваники. 9- }$
Для гальванического покрытия металлического серебра анод представляет собой брусок металлического серебра, а электролит представляет собой раствор цианида серебра в воде, а для гальванопокрытия золота анод представляет собой золотой анод, а электролит представляет собой цианид золота.
Раствор, используемый при гальванопокрытии золота и серебра, представляет собой раствор $Na[Au{(CN)_2}]$ (ауроцианид натрия) и $Na[Ag{(CN)_2}]$ (серебристоцианид натрия).
В процессе золотого покрытия $Au(s)$ изделие, которое необходимо покрыть, выступает в качестве катода, а блок чистого металла выступает в роли анода, на котором будет выполняться гальваническое покрытие, и $Na[Au{(CN)_2} В этом процессе используется раствор ]$ (ауроцианида натрия)
В процессе покрытия серебром $Ag(s)$изделие, подлежащее покрытию, действует как катод, а блок чистого металла действует как анод, с помощью которого будет выполняться гальваническое покрытие, и $Na[Ag{(CN)_2} В этом процессе используется раствор ]$ (серебристоцианистого натрия).
Следовательно, правильный ответ — вариант D.
Примечание: Не путайте вариант B и вариант D. Оба электролита будут цианидными. Кроме того, цианид используется при гальванике золота и серебра, поскольку он предотвращает осаждение цианида серебра и соли цианида золота из раствора, обеспечивает электропроводность электролита и способствует растворению серебряных и золотых анодов.
Недавно обновленные страницы
Большинство эубактериальных антибиотиков получены из биологии ризобия класса 12 NEET_UG
Биоинсектициды саламин были извлечены из класса 12 Biology NEET_UG
Какое из следующих утверждений, касающихся Baculovirusses, NEET_UG
. Какое из следующих утверждений, касающихся Baculoviruses, NEET_UG
Какое из следующих утверждений, касающихся Baculoviruses, NEET_UG
. муниципальные канализационные трубы не должны быть непосредственно 12 класса биологии NEET_UG
Очистка сточных вод выполняется микробами A B Удобрения 12 класса биологии NEET_UG
Иммобилизация фермента – это конверсия активного фермента класса 12 биологии NEET_UG
Большинство эубактериальных антибиотиков получают из биологического класса Rhizobium 12 NEET_UG
Саламиновые биоинсектициды были извлечены из биологического класса А 12 NEET_UG
12 класс биологии NEET_UG
Канализационные или городские канализационные трубы не должны быть напрямую 12 класс биологии NEET_UG
Очистка сточных вод выполняется микробами A B Удобрения 12 класс биологии NEET_UG
Иммобилизация фермента — это адвокат активного фермента класса 12 Biology NEET_UG
Трендовые сомнения
ОБОЛЛЕДЕНИЯ различных металлов. Хорошая электропроводность, низкое контактное сопротивление, а также хорошая паяемость золота, золотые покрытия находят широкое применение в электронике и электротехнике.
 Типичная толщина слоя от нескольких сотен нм (например, для припоя) до нескольких мкм используется в качестве защиты от коррозии.
Типичная толщина слоя от нескольких сотен нм (например, для припоя) до нескольких мкм используется в качестве защиты от коррозии.
Щелочной цианид. Осаждение золота
В качестве электролита здесь используется высокотоксичный дицианоаурат(I) калия = K[Au(CN) 2 ]. Этот раствор содержит примерно 68% золота и диссоциирует в водном растворе на ионы K + и [Au(CN) 2 ] — . Последние мигрируют к аноду и диссоциируют там на ионы Au + и (CN) — . Ионы золота мигрируют обратно к катоду, где они нейтрализуются и осаждаются на катоде.
В качестве анода используются либо растворимые золотые или золото-медные электроды, либо нерастворимые покрытые платиной титановые электроды.
Нейтральный цианид для осаждения золота
Этот электролит также основан на дицианоаурате калия, но не содержит свободного цианида (без свободных ионов (CN) — ). В качестве анода используются нерастворимые покрытые платиной титановые электроды.
Кислотное цианидное осаждение золота
Источником золота в электролите также является дицианоаурат калия, который дополнительно содержит кобальт или никель, а также лимонную кислоту. В результате могут быть получены блестящие золотые слои, которые являются сравнительно твердыми из-за их относительно большой доли органических компонентов и имеют низкую пластичность.
В качестве анодов используется нерастворимый титан с платиновым покрытием или нержавеющая сталь.
Сильнокислотное цианидное осаждение золота
Для этой цели трехвалентный тетрацианоаурат(III) калия = K [Au(CN) 4 ], который также стабилен в сильнокислых растворах, образует металлическую поставку электролита . Кроме того, добавляют минеральные кислоты, такие как серная или фосфорная кислота.
Бесцианидное осаждение сульфитов золота
Вместо высокотоксичных цианосоединений электролит основан на дисульфитоаурате аммония(I) = (NH 4 ) 3 [Au(SO 3 ) 2 ] или дисульфитоаурате натрия(I) = ( Na) 3 [Au(SO 3 ) 2 ] (сульфит щелочного металла). Ионы [Au(SO 3 ) 2 ] 3- раствора распадаются вблизи катода на ионы Au + и (SO 3 ) 2-, ионы золота восстанавливаются до золота. на катод и осаждается.
Ионы [Au(SO 3 ) 2 ] 3- раствора распадаются вблизи катода на ионы Au + и (SO 3 ) 2-, ионы золота восстанавливаются до золота. на катод и осаждается.
В дополнение к отсутствию высокотоксичных цианидных ванн, слои золота, осажденные из сульфитных электролитов, обладают преимуществами отличной макрорассеивающей способности (= высокая скорость осаждения также в местах ослабления тока электрода) и высокой пластичности.
По этой причине наша золотая ванна NB SEMIPLATE AU 100 основана на сульфитном электролите.
Формирование глянца
Высокий блеск напыленного золота требует гладкой поверхности с тонкой четкой кристаллической структурой. Для этого необходимо способствовать образованию зародышей при росте золота и в то же время подавлять рост кристаллов.
Это требование выполняется, в зависимости от электролита, добавлением таких элементов, как мышьяк, таллий, селен и свинец, а также этилендиамин, которые контролируют рост кристаллитов с помощью локальной селективной пассивации или химической буферизации непосредственно в место залегания золота.
Никелирование
Никелирование сульфатом никеля
Основным поставщиком металла является сульфат никеля в виде гексагидрата с формулой NiSO 4 ·(H 2 O) 6 или в виде гептагидрата (NiSO 4 ·(H 2 O) 7 ). Хлорид никеля в виде гексагидрата = NiCl 2 · (H 2 O) 6 служит для улучшения растворимости анода, а также в качестве проводящей соли для увеличения электропроводности электролита. Борная кислота (H 3 BO 3 ) служит химическим буфером для поддержания значения pH.
Сульфат никеля диссоциирует в водном растворе на Ni 2+ и (SO 4 ) 2- ионов. Ионы Ni 2+ восстанавливаются до никеля на катоде, который осаждается там в виде металлического покрытия. Ионы сульфата мигрируют к медному аноду и образуют там новый сульфат меди, который растворяется в растворе, потребляя анод.
Осаждение никеля хлоридными электролитами
Чистые (т.е. не содержащие сульфата никеля) хлоридные электролиты состоят из NiCl 2 ·(H 2 O) 6 в качестве поставщика металла и проводящей соли в одном, и борной кислоты в качестве химического буфера.
По сравнению с электролитами на основе сульфата никеля, ванны с хлоридом никеля обеспечивают осаждение с меньшей электрической мощностью из-за их более высокой электропроводности. Однако ванны с хлоридом никеля дороже и более агрессивны, чем ванны с сульфатом никеля.
Осаждение никеля сульфаматом никеля
Основным поставщиком металла для этого электролита является 4-гидрат сульфамата никеля с формулой Ni(SO 3 NH 2 ) 2 ·(H 2 O) 4 , хлорид никеля = NiCl 2 для улучшения растворимости анода и борная кислота химическая (H 8 как BO 0 819081 буфер для поддержания значения рН.
Сульфамат никеля диссоциирует в водном растворе на ионы Ni 2+ и (SO 3 NH 2 ) 2-. Ионы Ni 2+ восстанавливаются до никеля на катоде, который осаждается там в виде металлического покрытия. Ионы сульфата мигрируют к никелевому аноду и образуют там новый сульфамат никеля, потребляя анод.
Сульфамат никеля обладает очень высокой растворимостью в воде, так что можно приготовить очень богатые металлом ванны с высокой плотностью тока и скоростью осаждения, которые, тем не менее, позволяют получить слои никеля с хорошими механическими свойствами. Использование электролита на основе сульфамата никеля особенно рекомендуется, когда одновременно требуются толстые и ненапряженные слои. Наплавленный слой никеля очень пластичен и обеспечивает хорошую защиту от износа и коррозии.
По этой причине наша никелевая ванна NB SEMIPLATE AU 100 основана на электролите на основе сульфамата никеля.
Необходимые условия для блестящих никелевых пленок
Какие свойства поверхности приводят к блестящей (никелевой) поверхности для никеля еще не полностью изучены, даже если очень гладкая мелкокристаллическая структура играет важную роль.
Мелкокристаллическая поверхность требует, с одной стороны, высокой плотности зародышей, с другой стороны, подавления роста этих зародышей в более крупные кристаллиты.
Осветлитель (основные отбеливатели)
Добавки, такие как сульфонамиды, сульфонимиды и сульфоновые кислоты, вызывают измельчение зерна растущего слоя никеля, который обычно имеет высокую пластичность.
Осветлители и выравниватели (вторичные осветлители)
Осветлители и выравниватели в качестве добавок делают слои блестящими, хотя и менее пластичными.
Олово
Осаждение олова сульфатом олова(II)
Здесь раствор электролита состоит из сернокислого сульфата олова(II). Сульфат олова диссоциирует в водном растворе на Sn 2+ и (SO 4 ) 2- ионов. Ионы Sn 2+ восстанавливаются до олова на катоде, которое осаждается там в виде металлического покрытия. Ионы сульфата мигрируют к оловянному аноду и образуют там новый сульфат олова, который растворяется в растворе, потребляя анод.
Осаждение олова сульфатом олова(II)-метан
Здесь электролит состоит из метансульфокислоты (CH 3 SO 3 H) и ее соли, сульфоната олова(II)-метана. Эта соль диссоциирует в водном растворе до Sn 2 + и (CH 3 SO 3 ) 2- ионы. Ионы Sn 2+ восстанавливаются до олова на катоде, которое осаждается там в виде металлического покрытия. Ионы сульфата метана мигрируют к оловянному аноду и образуют там новый сульфат олова(II)-метан, который растворяется в растворе, потребляя анод. Наш оловянный электролит NB SEMIPLATE SN 100 основан на сульфонате олова(II)-метан и метансульфоновой кислоте.
Медное покрытие
Области применения
В электронике электрохимическое меднение используется, среди прочего, для изготовления печатных плат, а также сквозных соединений.
Щелочные цианидные отложения меди
В данном случае металл-носитель — цианид меди(I) (CuCN), растворимый не в воде, а в водных растворах NaCN или KCN, с образованием растворимых цианидных комплексов через
CuCN + 2 NaCN → Na 2 [Cu(CN) 3 ].
Наплавленные медные слои имеют очень хорошую адгезионную прочность.
Сернокислое осаждение меди
В качестве альтернативы высокотоксичному цианиду меди(I) электролит для сернокислотного осаждения состоит из сульфата меди (CuSO 4 ), растворенного в разбавленной серной кислоте. Сульфат меди диссоциирует на ионы Cu 2+ и (SO 4 ) 2- в водном растворе. Медь 9Ионы 0082 2+ восстанавливаются на катоде до меди, которая осаждается там в виде металлического покрытия. Ионы сульфата мигрируют к медному аноду и образуют там новый сульфат меди, который растворяется в растворе, потребляя анод.
Серная кислота служит не только для улучшения электропроводности электролита, но и является необходимым условием для когерентного однородного осаждения слоев.
Наша никелевая ванна NB SEMIPLATE CU 100 изготовлена из сульфата меди, растворенного в разбавленной серной кислоте.
Гальваническое осаждение серебра
Области применения
В (микро)электронике слои серебра используются из-за их хороших электрических свойств: среди всех металлов серебро обладает самой высокой электропроводностью.
 Существует два метода нанесения покрытий: электрохимический и химический. Разница…
Существует два метода нанесения покрытий: электрохимический и химический. Разница…